Fabricación de biomateriales compuestos para su aplicación como implante óseo
José Alanís, profesor de Ingeniería de la Universidad Anáhuac Querétaro, nos comparte un interesante artículo sobre biomateriales.
La revista +Ciencia de la Facultad de Ingeniería nos trae un interesante artículo de José Rafael Alanís Gómez, profesor de la Facultad de Ingeniería de la Universidad Anáhuac Querétaro, quien se enfoca en los biocompuestos como materiales utilizados para el reemplazo óseo, formados por una matriz y un refuerzo de fibras naturales.
Fabricación de biomateriales compuestos para su aplicación como implante óseo
Resumen
Los biocompuestos son estudiados frecuentemente debido a la respuesta favorable que presentan cuando son utilizados en la sustitución de tejido óseo. Para que puedan utilizarse como reemplazo de tejido óseo humano es importante que tengan una morfología, tamaño y composición química similar a la que muestran estando presentes en dicho tejido; de este modo, obtienen una mayor probabilidad de aceptación por parte del organismo receptor. Además, el material de reemplazo óseo debe poseer propiedades mecánicas similares al tejido duro, como elasticidad, resistencia a la compresión y flexibilidad, para que el individuo que ha recibido un implante de este tipo, pueda llevar a cabo actividades cotidianas comunes. Paralelamente, el material de reemplazo óseo debe ser lo suficientemente poroso para permitir que los fluidos y células encargadas de la regeneración del tejido óseo puedan llevar a cabo su labor, permitiendo con ello el restablecimiento natural del hueso y, al mismo tiempo, el paso de nutrientes necesarios para sus funciones biológicas. Es por eso que en este artículo se revisarán los métodos de síntesis de biocompuestos, desde la materia prima hasta su moldeado.
Introducción
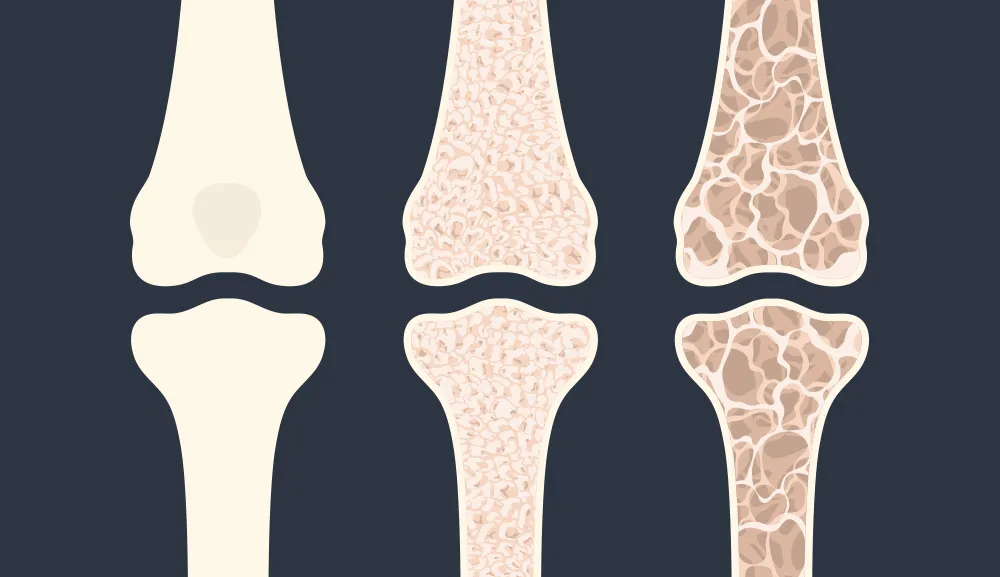
La osteoporosis es una patología que afecta a los huesos y es provocada por la disminución del tejido que los forma, tanto de las proteínas que constituyen su matriz o estructura como de los componentes minerales de calcio que contienen. Como consecuencia de ello, el hueso es menos resistente y más frágil de lo normal, tiene baja resistencia al impacto y se rompe con relativa facilidad tras un traumatismo, produciéndose fracturas o microfracturas.
De acuerdo con el estudio Auditoría latinoamericana: epidemiología, costos e impacto de la osteoporosis en 2012, de la Fundación Internacional de Osteoporosis, el riesgo de sufrir una fractura de cadera a los 50 años en México, se estima de 8.5% en las mujeres y 3.8% en los hombres. En otras palabras, una de cada 12 mujeres y uno de cada 20 hombres mayores de 50 años sufrirán una fractura de cadera en la edad adulta.
El costo total directo de las fracturas de cadera estimado para 2006, según la incidencia anual proyectada de las fracturas de cadera en México, superó levemente los 97 millones de dólares. Este cálculo se basó en la existencia de casi 22,000 casos de fracturas de cadera, con un costo individual por evento de 4,365.50 dólares, y se estima que la tendencia de las fracturas irá en aumento.
Tomando en cuenta lo anterior, es claro que las oportunidades de mercado para nuevos desarrollos en el área de los biomateriales son muy promisorias, por lo que es necesario la expansión de tecnologías nacionales para la producción de biomateriales con aplicaciones en el área de la salud. La mayor parte de los biomateriales que se consumen en México son de importación.
Antecedentes y marco teórico
El tejido óseo es un tejido conjuntivo que se caracteriza por tener una matriz extracelular mineralizada. La característica que distingue el tejido óseo de los otros tejidos conjuntivos es la mineralización de su matriz, que produce un tejido muy duro capaz de proveer sostén y protección. El mineral es fosfato de calcio en la forma de cristales de hidroxiapatita (HAp).
Los biomateriales que se utilizan para su aplicación en tejidos óseos los podemos dividir en: matriz extracelular, polímeros naturales y artificiales, biocerámicas, biocristales y biocompuestos.
En este artículo nos enfocaremos en los biocompuestos, que son materiales formados por una matriz y un refuerzo de fibras naturales. Este tipo de materiales a menudo imitan la estructura de los tejidos vivos y, generalmente, la fase de la matriz está formada por polímeros naturales y/o sintéticos. La matriz es importante para proteger las fibras de la degradación ambiental, así como para mantenerlas juntas y transferir las cargas sobre todo el material. Mientras que la fase inorgánica más utilizada es la HAp, debido a que es la que se encuentra presente en el tejido óseo.
Desde hace muchos años, la obtención de HAp sintética ha sido objeto de estudio de varios investigadores. La razón principal reside en que es un material bioactivo y tiene una composición química similar a la del componente inorgánico de los tejidos óseos naturales.
La HAp puede ser sintetizada mediante diferentes rutas químicas, utilizando soluciones precursoras sometidas a altas condiciones de presión y temperatura, con ello se obtienen materiales cuyas propiedades físicas y químicas son diversas, con características morfológicas controladas; además de alta pureza, composición homogénea y tamaños de partícula nanométricos.
Sin embargo, para que una cerámica de HAp funcione de manera adecuada como biomaterial, debe ser lo suficientemente porosa para permitir el paso de fluidos y el suministro de nutrientes; asimismo, propiciar la penetración celular y la incursión vascular rápida, lo que podría favorecer el crecimiento de tejido óseo natural, con lo que se llevaría a cabo una regeneración del tejido óseo dañado. Así pues, el control de la porosidad a escalas meso, micro y macroscópicas es fundamental en el desarrollo de nuevas biocerámicas y sus aplicaciones.
Entonces, el material de reemplazo óseo deberá poseer una morfología, porosidad y resistencia a la compresión semejantes al tejido óseo humano; así, obtendrá una mayor probabilidad de aceptación por parte del organismo receptor. Dichas propiedades están directamente relacionadas con la composición química y la estructura que posea el biocerámico.
Desarrollo
De acuerdo con lo antes mencionado, se estudiarán los métodos que existen de síntesis de HAp y los métodos de moldaje para su utilización como reemplazo óseo.
Síntesis de HAp
La HAp se puede sintetizar por diferentes métodos, que pueden dividirse en métodos secos, húmedos y de energía alterna. La preparación de HAp para el método de la ruta en seco consiste en un tratamiento térmico a precursores finamente triturados; el requisito esencial es tener una mezcla que sea perfectamente homogénea. La pureza del producto final puede ser afectada por el pesado de la preparación; además, requiere al-tas temperaturas, lo que afecta la resistencia mecánica.
En cuanto a los métodos húmedos, son bastante utilizados porque permiten un perfecto control sobre la estructura, textura y morfología, y conducen a un alto rendimiento de HAp. Su inconveniente estriba en que, a veces, dan lugar a estructuras que no son cristalográficamente puras; otras fases de fosfatos están presentes con HAp. Los métodos húmedos más utilizados son el hidrotermal y el Sol-Gel.
En el método hidrotermal la reacción se produce en presencia de agua, a una temperatura y presión relativamente altas. Los reactivos se calientan en un sistema sellado, en el que la mezcla reaccionante se presuriza a medida que se calienta continuamente; sin embargo, como se dijo anteriormente, con este método se obtienen otras fases de fosfatos de calcio. Por su parte, el método Sol-Gel facilita la formación de cristales de HAp en condiciones de baja temperatura y presión, gracias a la alta reactividad de los reactivos, pero además de obtener otras fases de fosfato de calcio, la principal desventaja de este método es el tiempo, que es excesivamente largo.
A menudo, los métodos de energía alterna se combinan con otros métodos convencionales, con objeto de crear una sinergia entre las diferentes técnicas y así aumentar el rendimiento. Los métodos de este tipo más utilizados son el método Ball-Milling y los métodos asistidos por microondas.
El Ball-Milling ha sido ampliamente empleado en la síntesis de Hap, con ventajas como la simplicidad, la reproducibilidad y la producción a gran escala de HAp. El control del crecimiento de HAp mediante esta técnica depende estrechamente del tipo de reactivos empleados, del medio de molienda, del diámetro de las bolas de molienda, del tipo de atmosfera y de la duración de las etapas de molienda.
La síntesis de materiales a través de métodos asistidos por microondas tiene las ventajas de ofrecer un calentamiento homogéneo durante todo el volumen, así como una eficiente transformación de energía. La HAp sintetizada por este método es particularmente homogénea en términos de tamaño, porosidad y morfología. Además, agrega el beneficio de un rápido crecimiento, un tamaño de partícula pequeño y la distribución estrecha de tamaño de partícula debido a la rápida nucleación.

Moldeo del material poroso
El desarrollo de estructuras de materiales porosos para su utilización como reemplazo óseo está motivado para replicar la naturaleza del hueso natural. Dado que la porosidad está asociada tanto a las propiedades mecánicas del biomaterial, como al transporte de nutrientes dentro del mismo, se ha dedicado mucha atención a la fabricación de andamios porosos. A continuación, se describirán los métodos de fabricación de andamios porosos más comunes.
El moldeo de los andamios por Freeze Casting es un método simple, empleado originalmente para producir estructuras porosas complejas de componentes cerámicos o poliméricos; utiliza agua, camfeno y glicerol como disolventes. El vehículo disolvente que actúa como aglutinante mantiene intacta la suspensión, y el disolvente se retira de esta mediante sublimación por liofilización helada, dejando una red porosa interconectada. Posteriormente, se sinteriza a temperaturas apropiadas para proporcionar una mejor resistencia mecánica.
En el Gel Casting, se crea una suspensión cerámica concentrada mezclando un polvo cerámico y una solución de monómero. Después, esta suspensión se vierte en un molde en busca de obtener la forma deseada, y durante el calentamiento los monómeros se polimerizan con el fin de constituir una estructura de red. Luego, para obtener la parte cerámica pura, el disolvente de la suspensión de cerámica debe ser removido por secado en el aire. Por último, se sinteriza la suspensión y se obtiene la densidad completa del material cerámico.
Finalmente, con el avance de la tecnología, se han presentado más de veinte sistemas de prototipos rápidos con respecto a la ingeniería de tejidos duros. Los métodos más notables son la estereolitografía, el sinterizado selectivo por láser, el modelado de deposición, la impresión de cera y el bioplotador. La mayoría de estas impresiones 3D consisten en poner una capa del material a implantar y después fundir la parte superior, ya sea por láser, calor o CO2, para después poner la siguiente capa. Estos métodos permiten un control preciso no solo de la arquitectura del andamio, sino también del tamaño, forma, interconectividad, ramificación, geometría y orientación; además no incluyen disolventes orgánicos tóxicos.
Conclusión
Por lo que podemos ver, a pesar de que existen diferentes estudios acerca de cómo sintetizar materiales utilizados para el reemplazo óseo, todavía hay muchas áreas de oportunidades debido a que es un elemento biológico que debe de tener muchos cuidados; aunado a que su impacto en la economía y en la mejora de la salud es sustancial.
En mi opinión, el método de fabricación de la HAp que tiene ventaja sobre los demás es el hidrotermal asistido por microondas, porque permite un mejor control en la morfología y en la composición de la Hap; además, presenta un tiempo de reacción relativamente corto.
En cuanto al método de moldeado, los tres aquí referidos parecen ser buenas opciones y presentan algunas oportunidades de mejora. Por ejemplo, el método Frezee Casting registra un rango de porosidad variable debido a que es difícil controlar los disolventes. El Gel Casting tiene como desventaja la manipulación del mismo, pues antes de la adición de la fase orgánica el material es un tanto frágil.
El moldeado por prototipado rápido presenta una excelente y bien controlada porosidad, sin embargo, conlleva el problema de que es costoso y consume demasiado tiempo, porque los andamios son construidos capa por capa y las impresiones son personalizadas, lo que significa tiempo de diseño computacional; además, depende mucho de la disponibilidad de biomateriales con morfologías exactas.
*Colaboración José Rafael Alanís Gómez, profesor de la Facultad de Ingeniería de la Universidad Anáhuac Querétaro.
Referencias:
• Alanís, J. R., Rivera, E. M., Cervantes, J. S., Almanza, H., Nava, R., Cortés, C. y Velázquez-Castillo, R. (2016) Synthesis of Micro and Nano-Sized Hydroxyapatite Fibers Through the Microwave Assisted Hydrothermal Method. Journal of Nanoscience and Nanotechnology, 16(7), pp. 7557-7566.
• Arami, H., Mohajerani, M., Mazloumia, M., Khalifehzadeh, R., Laka, A. y Sadrnezhaad, S. K. (2008). Rapid For-mation of Hydroxyapatite Nanostrips Via Microwave Irradiation. Iran, Journal of Alloys and Compounds, 469, pp. 391-394.
• Chu, P. K. y Liu, X. (2008) Biomaterials Fabrication and Processing. Handbook, CRC Press. Fihri, A., Len, C., Varma, R. S. y Solhy, A. (2017) Hydroxyapatite: A Review of Syntheses, Structure and Applications in Heterogeneous Catalysis. Coordination Chemistry Reviews.
• Guo, X. (2011) Gel Casting of High Strength Ceramics. Chalmers University of Technology. Johansson, H., Clark, P., Carlos, F., Oden, A., McCloskey, E. V. y Kanis, J. A. (2011) Increasing Age-and Sex-Specific Rates of Hip Fracture in Mexico: A Survey of the Mexican Institute of Social Security. Osteoporos Int. Aug., 22(8), pp. 2359-2364.
• Mallick, K. K. y Cox, S. C. (2013) Biomaterial Scaffolds for Tissue Engineering. Frontiers in Bioscience (Elite edition), 5, pp. 341-360.
• Mohanty, A. K., Misra, M. y Drzal, L. T. (2005) Natural Fibers, Biopolymers, and Biocomposites. CRC press. Rivera, E. M., Velázquez, R. y Cabrera, J. L. (2010) Mor phological Analysis of Hydroxyapatite Particles Obtai-ned by Different Methods. Materials Science Forum, vols. 638-642, pp. 681-686.
• Ross, M. H. y Pawlina, W. (2013) Histología: texto y atlas color con biología celular y molecular, 6.a ed., pp. 218-230. Valeri, S. G. y Aleksandra, C. (2012) Hydroxyapatite: Synthesis, Properties and Applications. Chapter 2. Nova Sciences Pub., pp. 91-132.
• Zakaria, S. M., Sharif Zein, S. H., Othman, M. R., Yang, F. y Jansen, J. A. (2013) Nanophase Hydroxyapatite as a Bio-material in Advanced Hard Tissue Engineering: A Review. Tissue Engineering Part B: Reviews, 19(5), pp. 431-441.
• Zanchetta, J. y MacDonald, S. (2012) The Latin America. Regional Audit. Epidemiology, Costs & Burden of Os-teoporosis in 2012.
La revista +Ciencia de la Facultad de Ingeniería contiene interesantes artículos como El Cascajo: recuperación de hábitats naturales, rehabilitación al alcance de tu mano, campana de flujo laminar, fabricación de bocinas caseras para tu celular, entre otros interesantes temas.
Da clic en la imagen para conocer la revista completa

Para más artículos interesantes como este, te invitamos a consultar +Ciencia, la revista cuatrimestral de la Facultad de Ingeniería, que en cada número tiene contenido relevante de sus alumnos e investigadores. Da clic aquí para conocer todas las ediciones.
Más información:
+Ciencia. Revista de la Facultad de Ingeniería
Dra. María Elena Sánchez Vergara
elena.sanchez@anahuac.mx
